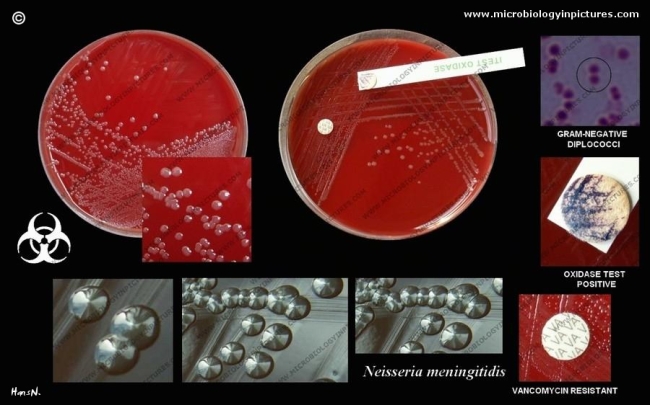
Estreptococos
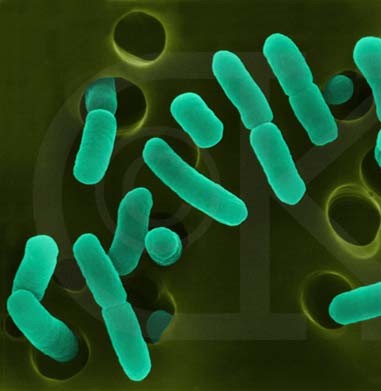
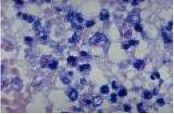
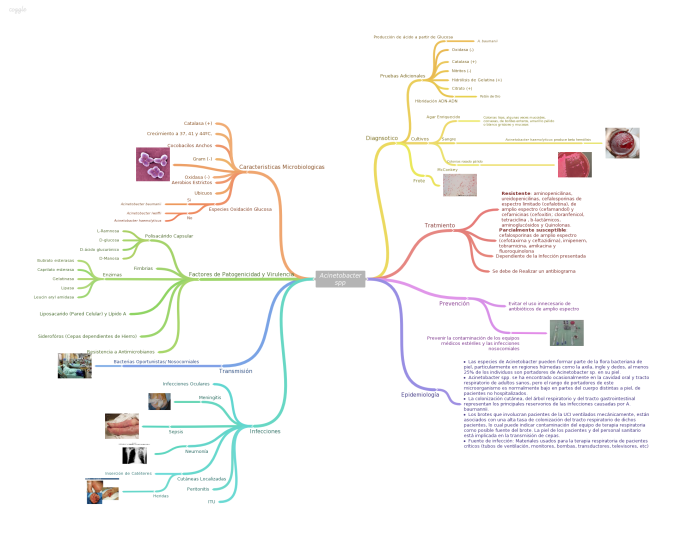
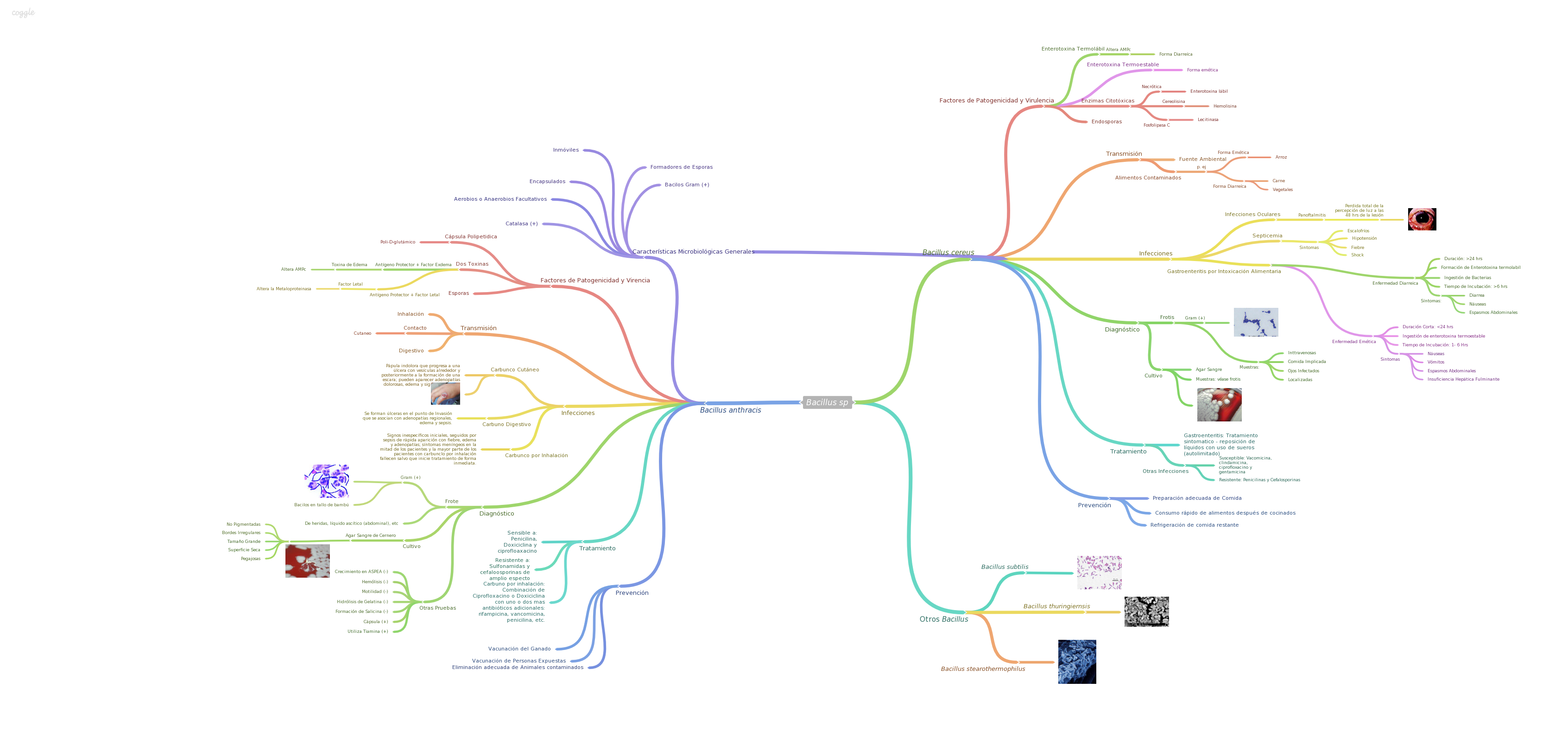
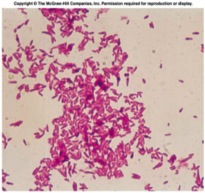
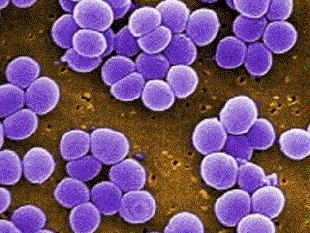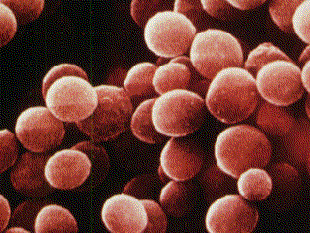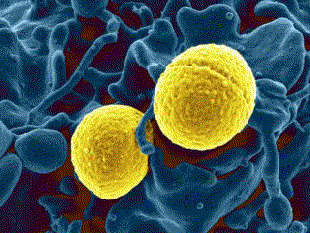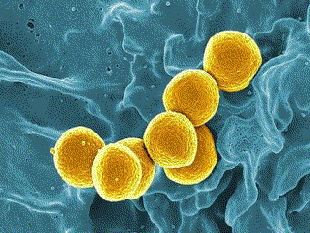
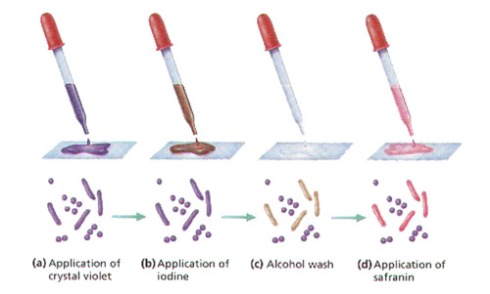
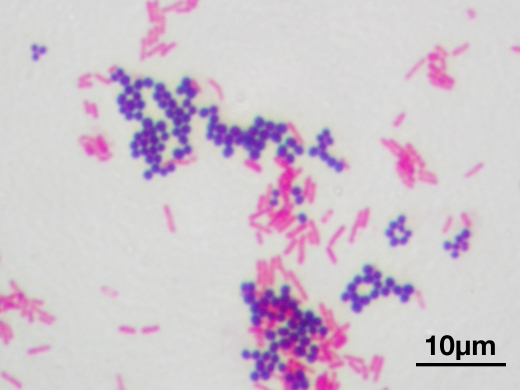
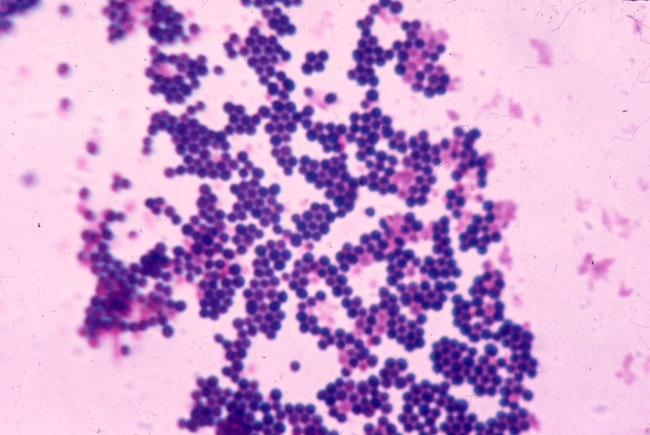
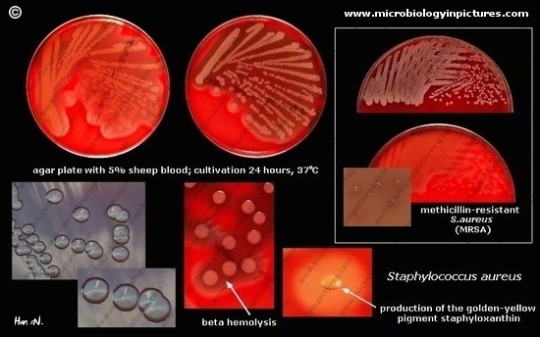
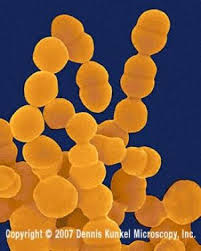
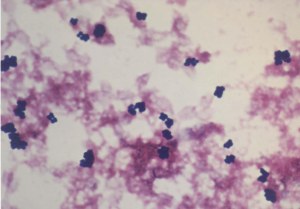
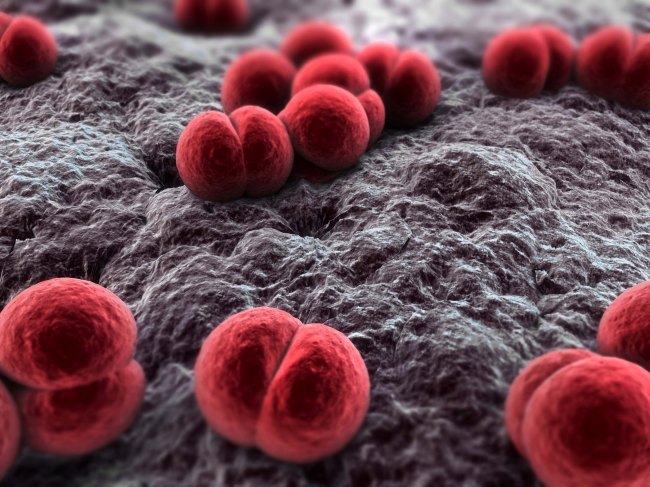
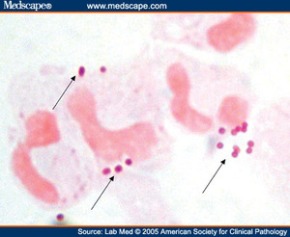
Los estreptococos son bacterias esféricas grampositivas que de manera característica forman pares o cadenas durante su multiplicación. Los estreptococos son anaerobios facultativos, catalasa (-), muchos estreptococos pueden producir hemolisis de los eritrocitos in vitro en grados variables. La destrucción completa de los eritrocitos con el aclaramiento de la sangre alrededor del crecimiento bacteriano se denomina hemolisis beta. La lisis incompleta de los eritrocitos con reducción de hemoglobina y la formación de pigmento verde se llama hemolisis alfa. Otros estreptococos son no hemolíticos (a veces denominada hemolisis gamma). Tienen una amplia distribución en la naturaleza. Algunos son de la microbiota normal de los seres humanos, otros están relacionados con enfermedades humanas importantes atribuibles en parte a la infección por estreptococos y en parte a la sensibilización a ellos. Los estreptococos elaboran diversas sustancias y enzimas extracelulares. Los estreptococos son de la familia Streptococcaceae, su genero se denomina Streptococcus. Los estreptococos se clasifican según en grupos según sus antígenos de superficie, estos grupos contienen una variedad de tipos de proteínas. Muchos estreptococos producen capsulas como los del grupo A (acido hialuronico), se pueden clasificar las colonias por su morfología ya sea esta colonia mucoide por cepas que producen capsulas grandes, abundante gel de acido hialuronico que se presentan como brillantes y acuosas. Están las colonias mate, que son mas planas y mas rugosas (deshidratadas) y las colonias brillantes que son mas pequeñas. Los estreptococos agrupables son los A, B y D (mas frecuentes) y los grupos C, G y F (menos frecuentes), los no agrupables son los Streptococcus pneumoniae (que produce neumonía) y los Streptococcus viridans (S. Mutans que causan caries dental) La clasificación esta dada gracias a Rebecca Craighill Lancefield. La microbióloga fue quien agrupó los estreptococos beta hemoliticos en grupos inmunológicos por sus antígenos de pared celular o de la capsula. Se ha estudiado 20 grupos: A-H y K-V. Algunas especies no son agrupables, algunas especies pertenecen a varios grupos y un grupo puede tener diferentes especies.
Streptococcus pyogenes
Familia: Streptococcaceae
Genero: Streptococcus
Nombre científico: Streptococcus pyogenes
Nombre común: Estreptococo pyogenes
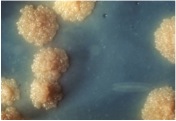
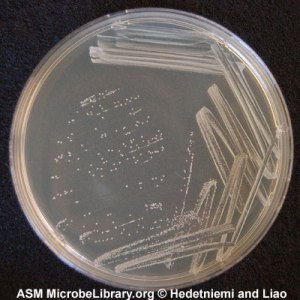
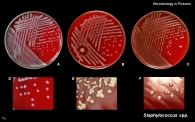
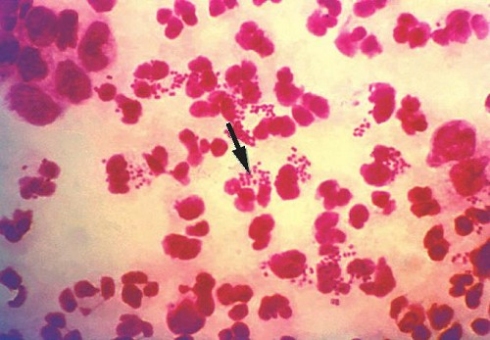
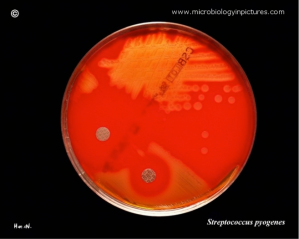
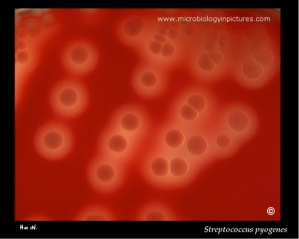
Fisiología microbiana: Es el principal microorganismo patógeno humano que produce invasión local o sistémica y trastornos inmunitarios posestreptocócicos. Suelen ser suceptibles a la bacitracina. Afecta a todas las edades con una incidencia entre 5 y 15 años. Los aislamientos de S. Pyogenes son cocos esféricos de 0,5 a 1,0 mm que forman cadenas cortas en las muestras clínicas y cadenas mas largas cuando crecen en medio de cultivo. El crecimiento es óptimo en un medio de agar sangre enriquecido, pero se inhibe si el medio contiene una concentración elevada de glucosa. Después de 24 horas de incubación se observan colonias blancas de 1 a 2 mm con grandes zonas de Beta hemólisis. Las cepas encapsuladas pueden presentar una apariencia mucoide en los medios recién preparados pero pueden estar arrugadas en los medios secos. Las colonias no encapsuladas son pequeñas y brillantes. El marco estructural básico de la pared celular es la capa de peptidoglicanos, que tiene una composición parecida a las de las bacterias grampositivas.
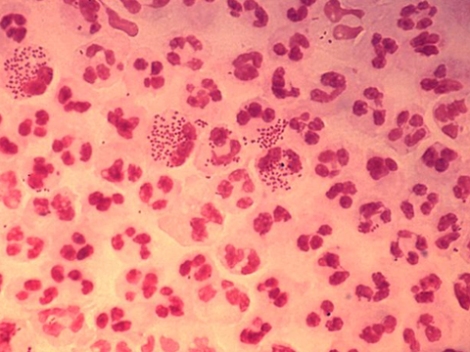
Factores de patogenicidad y virulencia: Las adhesinas se encuentran presentes en las fimbrias en la parte externa de la pared celular, estas se adhieren al epitelio respiratorio via fibronectina, el factor F es una proteína de unión a la fibronectina. Evasion de la fagocitosis: Proteina M, se une al fibrinógeno y bloquea la unión del complemento al peptidoglicano, esta sustancia es un factor de virulencia importante de Streptococcus pyogenes del grupo A, cuando está presente la proteína M, los estreptococos son virulentos y si no hay anticuerpos específicos tipo M, pueden resistir la fagocitosis a cargo de los leucocitos polimorfonucleares. La estreptolisina es destruida por el oxigeno atmosférico y solo puede demostrarse en colonias profundas. La estreptolisina S es estable al oxigeno y es la responsable de la hemolisis superficial de la colonia. En la fiebre escarlatina está presente la toxina pirogenica. La estreptoquinasa activa el plasminogeno, digiere fibrina y otras proteínas. La hialuronidasa rompe el acido hialuronico del tejido conectivo. La estreptodornasa despolimeriza el ADN.
Patogenia
Diversos procesos patológicos distintivos se relacionan con las infecciones por Streptococcus pyogenes, estas se pueden clasificar en 4 tipos: A, B , C y D
La categoría A responde a Enfermedades atribuibles a la invasión por Streptococcus pyogenes y estreptococos hemolíticos beta del grupo A.
La puerta de entrada determina el cuadro clínico principal. Sin embargo, en cada caso hay una infección difusa que se propaga con rapidez y que afecta los tejidos y se extiende por los conductos linfáticos produciendo solo una supuración local minima. Desde los linfáticos, la infección puede extenderse hacia la circulación sanguínea.
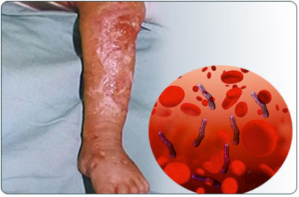
Erisipela: Si la puerta de entrada es la piel, sobreviene erisipela, con edema engrosado masivo y un margen de infección que avanza rápidamente.
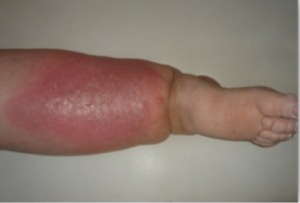
Celulitis: La celulitis estreptococia es una infección aguda de diseminación rápida de la piel y los tejidos subcutáneos. Se presenta tras la infección relacionada con traumatismos leves, quemaduras, heridas o incisiones quirúrgicas. Se presenta dolor, hipersensibilidad, edema y eritema. La celulitis se distingue de la erisipela por dos manifestaciones clínicas: en la celulitis, la lesión no está elevada y no esta bien definida la línea entre el tejido afectado y sano.
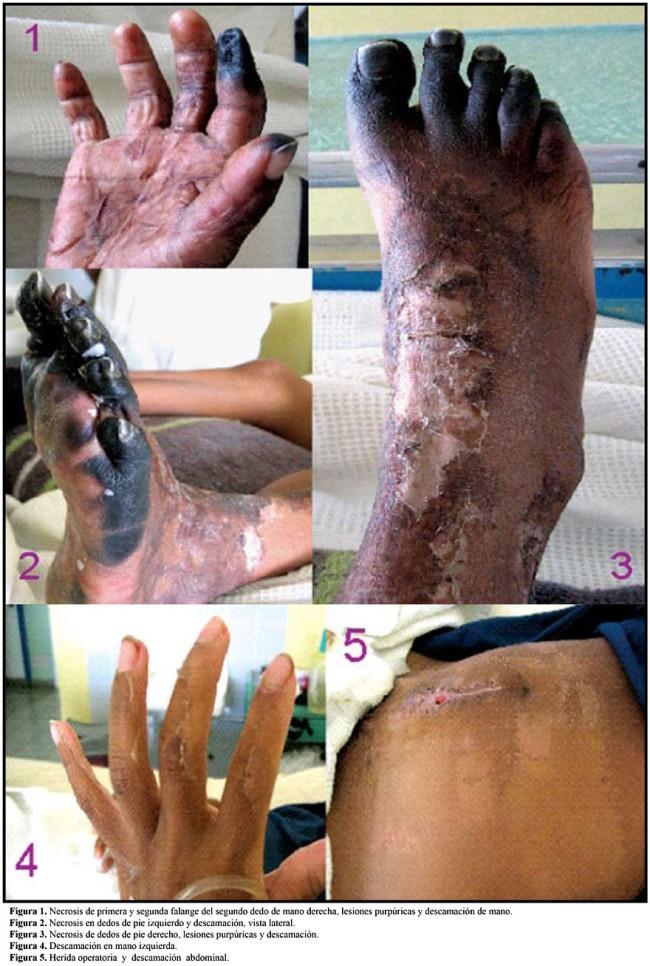
Fascitis necrosante (gangrena estreptocócica): Esta es una infección de los tejidos subcutáneos y la fascia. Hay necrosis considerable y de diseminación muy rápida de la piel y tejidos subcutáneos. Otras bacterias del Streptococcus pyogenes también causan fascitis necrosante. Los estreptococos del grupo A que producen fascitis necrosante a veces también se han denominado “bacterias comedoras de carne”.
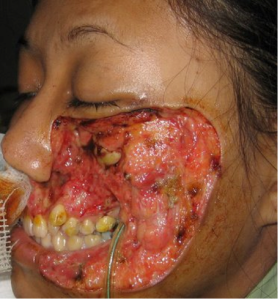
Fiebre puerperal: Los estreptococos entran en el útero después del parto, sobreviene fiebre puerperal, que es una septicemia que se origina en la herida infectada (endometritis).
Bacteriemia/septicemia: La infección de las heridas traumáticas o quirúrgicas por estreptococos produce bacteriemia, la cual rápidamente puede ser mortal. La bacteriemia por Streptococcus pyogenes también puede presentarse tras infecciones cutáneas como celulitis y pocas veces faringitis.
La categoría B representa a las enfermedades atribuibles a la infección local por Streptococcus pyogenes y sus productos derivados.
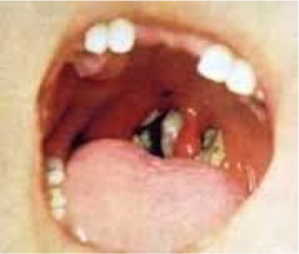
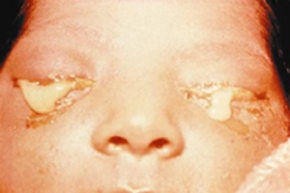
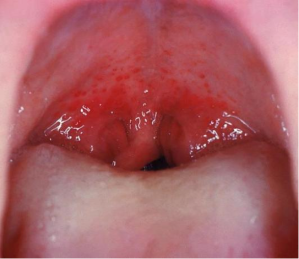
Faringitis estreptocócica: La infección mas frecuente debida a Streptococcus pyogenes beta hemolítico es la faringitis estreptocócica. El Streptococcus pyogenes se adhiere al epitelio faríngeo por medio de fimbrias superficiales cubiertas de acido lipoteicoico y también por acido hialuronico en las cepas encapsuladas. En los lactantes y en los niños pequeños, la faringitis ocurre como una rinofaringitis subaguda con una secreción serosa liquida y poca fiebre pero con tendencia de la infección a extenderse hacia el oído medio y la apófisis mastoides. Los ganglios linfáticos cervicales suelen estar aumentados de tamaño. La enfermedad puede persistir durante semanas. En los niños mayores y en adultos la enfermedad es mas aguda y se caracteriza por rinofaringitis intensa, amigdalitis e hiperemia intensa y edema en las mucosas, con exudado purulento, adenomegalia cervical dolorosa y por lo general fiebre alta. El 20% de las infecciones es asintomático. Puede presentarse un cuadro clínico similar con la mononucleosis infecciosa, la difteria, una infección gonocócica y la infección por adenovirus.
La infección de las vías respiratorias altas por Streptococcus pyogenes por lo general no afecta a los pulmones. Cuando se presenta neumonía, progresa rápido y es grave, lo mas frecuente es que sea una secuela de infecciones virales, por ejemplo, influenza o sarampión, que al parecer intensifican considerablemente la susceptibilidad.
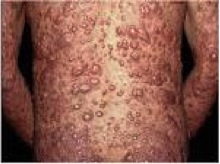
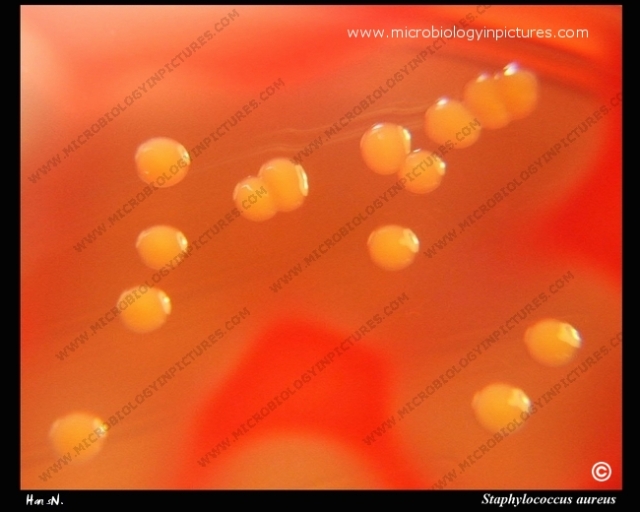
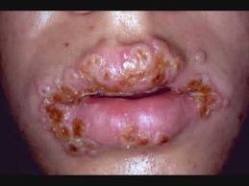
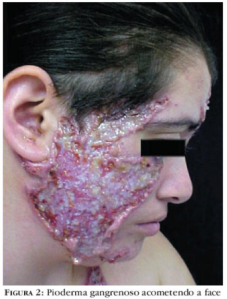
Piodermia estreptocócica: La infección local de las capas superficiales de la piel, sobre todo en los niños se denomina impétigo. Consta de vesículas superficiales que se rompen y de zonas erosionadas cuya superficie desollada está cubierta de pus para luego encostrarse. Se disemina por continuidad y es muy contagiosa sobre todo durante los climas húmedos calientes. Ocurre una infección mas generalizada en la piel eccematosa o herida o en las quemaduras y puede avanzar a la celulitis. Las infecciones cutáneas por estreptococos del grupo A suelen ser atribuibles a los tipos M 49, 57, 59 y 61 y pueden anteceder a la glomerulonefritis pero a menudo no originan fiebre reumática. El Staphylococcus aureus puede provocar una infección que es idéntica desde el punto de vista clínico y a veces están presentes tanto S. pyogenes como S. aureus.
La categoría C representa a las infecciones invasivas por estreptococos del grupo A, síndrome de choque toxico estreptocócico y fiebre escarlatina.
Síndrome de choque toxico estreptocócico: Se caracteriza por choque, bacteriemia, insuficiencia respiratoria y falla de múltiple órganos. Ocurre el deceso en casi el 30% de los pacientes, las infecciones tienden a presentarse después de traumatismos leves en personas por lo demás sanas con múltiples variantes de infección de tejidos blandos. Estas comprenden fascitis necrosante, miositis e infecciones en otros tejidos blandos; la bacteriemia ocurre con frecuencia.
Fiebre escarlatina: Está relacionada con faringitis por Streptococcus pyogenes, hay un periodo de latencia de una a cuatro semanas, después de lo cual a veces se presenta nefritis o fiebre reumática. El periodo de latencia indica que estas enfermedades posestreptocócicas no son atribuibles al efecto de la bacteria diseminada, mas bien representan una respuesta de hipersensibilidad. La nefritis mas a menudo va precedida de una infección de la piel; la fiebre reumática con mas frecuencia va precedida de una infección del sistema respiratorio.
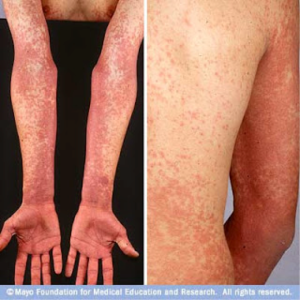
La categoría D responde a las enfermedades posestreptococicas (fiebre reumática y glomérulonefritis)
Glomerulonefritis: A veces se presenta de una a cuatro semanas después de una infección cutánea por S. pyogenes (pioderma, impétigo). Es posible que la glomerulonefritis se inicie por complejos de antígeno-anticuerpo que se depositan en la membrana basal glomerular. El antígeno mas importante probablemente está en la membrana del protoplasto estreptocócico. En la nefritis aguda, hay sangre y proteína en orina, edema, hipertensión arterial y retención de nitrógeno de urea; las concentraciones de complemento en suero también son bajas. Pocos pacientes fallecen; algunos presentan glomérulonefritis crónica con insuficiencia renal al final y la mayoría se restablece por completo.
Fiebre reumática: Ésta es la secuela mas grave de la infección por S. pyogenes pues produce lesión del musculo y las válvulas del corazón. El inicio de la fiebre reumática suele ir precedido de infección por S. pyogenes una a cuatro semanas antes, aunque la infección puede ser leve y es posible que no se detecte. Sin embargo, en general, los pacientes con faringitis estreptocócicas mas graves tienen una mayor posibilidad de presentar fiebre reumática. Los signos y síntomas caracteristicos de la fiebre reumática comprende fiebre, ataque al estado general, poliartritis migratoria no purulenta y signos de inflamación de todas las capas del corazón (endocardio, miocardio, pericardio). Es característico que la carditis produzca engrosamiento y deformación de las válvulas y que ocasione granulomas perivasculares pequeños en el miocardio (cuerpos de Aschoff) que finalmente son remplazados por tejido cicatrizal. Por tanto es, es importante proteger a estos pacientes de las infecciones recidivantes por S. pyogenes mediante la administración profiláctica de penicilina.
Epidemiologia
Los estreptococos del grupo A colonizan normalmente la orofaringe de los niños sanos y de los adultos jóvenes. Aunque se considera que la incidencia del estado de portador es del 15 al 20%, estos datos son equívocos. Se necesitan técnicas de cultivo muy selectivas para detectar un pequeño número de microorganismos en la secreciones orofaríngeas. Además, se había asumido que la colonización con streptococos del grupo A era sinónimo de la colonización con S. Pyogenes. Sin embargo ahora se conoce que S. Anginosus puede tener el antígeno especifico de grupo A y estar presente en la orofaringe. No se cree que esta especie produzca faringitis. La colonización con S. Pyogenes es transitoria, regulada tanto por la capacidad de la persona para desarrollar una inmunidad específica frente a la proteína M de la cepa colonizadora, como a la presencia de microorganismos competitivos en la orofaringe. Los pacientes no tratados producen anticuerpos frente a la proteína M bacteriana específica, lo que puede dar como resultado una inmunidad que dure toda la vida; sin embargo, en los pacientes tratados, esta respuesta de anticuerpos está disminuida. Las bacterias como los estreptococos a-hemolíticos y no hemolíticos son capaces de producir unas sustancias de tipo anticuerpo conocidas como bacteriocinas, que suprimen el crecimiento de los estretococos del grupo A. En general la enfermedad S. Pyogenes está producida por cepas de adquisición recientes que causan una infección de la faringe o de la piel antes deque se produzcan anticuerpos específicos o de que sean capaces de proliferar los microorganismos competitivos. La faringitis producida por S. Pyogenes es una enfermedad fundamentalmente de niños entre 5 y 15 años, aunque los lactantes y los adultos también son susceptibles. El patógeno se extiende de persona a persona a través de gotitas respiratorias. El hacinamiento, como en el caso de las aulas y las guarderías, aumenta las oportunidades que tiene el microorganismo de diseminarse, fundamentalmente en los meses de invierno. Las infecciones de los tejidos blandos (por ejemplo Hypoderma, erisipela, celulitis, fascitis) se ven producidas por una colonización inicial de la piel con estreptococos del grupo A, después de la cual los microorganismos se introducen en los tejidos superficiales o profundos a través de una solución de continuidad en la piel.
Tratamiento:
Todos los microorganismos de la especie Streptococcus pyogenes son susceptibles a la penicilina G y la mayoría a la eritromicina. Algunos son resistentes a las tetraciclinas. Los antimicrobianos no tienen ningún efecto sobre la glomerulonefritis y la fiebre reumática establecidas. Sin embargo, en las infecciones estreptocócicas agudas se debe hacer todo lo posible por erradicar con rapidez los estreptococos del paciente, eliminar el estimulo antigénico (antes del dia 8) y, por tanto, prevenir la enfermedad posestreptococica. Las dosis de penicilina o eritormicina que producen concentraciones eficaces en los tejidos durante 10 dias suelen lograr esto. Los antimicrobianos también son muy útiles para prevenir la reinfección por estreptococos beta hemolíticos del grupo A en los pacientes con fiebre reumática.
Ilustraciones:
Links
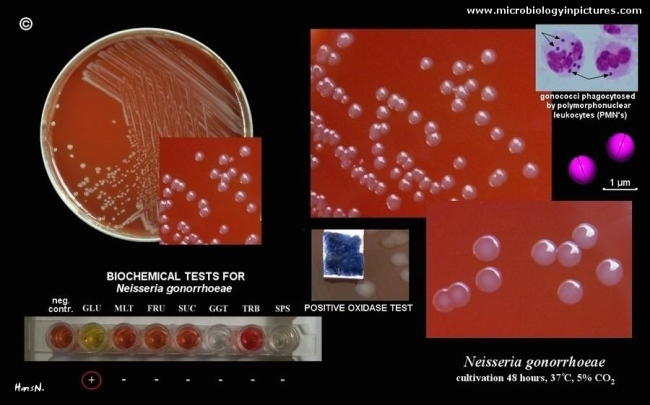
Microbiología en fotos: Streptococcus pyogenes http://www.microbiologyinpictures.com/streptococcus%20pyogenes.html
Manual de Merck: fascitis necrotizante
http://www.merckmanuals.com/professional/dermatologic_disorders/bacterial_skin_infections/necrotizing_subcutaneous_infection.html?qt=streptococcus%20pyogenes&alt=sh
Streptococcus agalactiae
Familia: Streptococcaceae
Genero: Streptococcus
Nombre científico: Streptococcus agalactiae
Nombre común: Estreptococo agalactiae
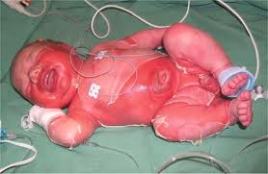
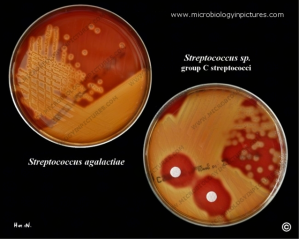
Fisiología microbiana: Estos son los estreptococos del grupo B. Es característico que sean beta hemolíticos y produzcan zonas de hemolisis que solo son un poco mayores que las colonias (1 a 2mm de diámetro). Los estreptococos del grupo B producen hidrólisis del hipurato de sodio y una respuesta positiva llamada CAMP. Los estreptococos del grupo B son parte de la microbiota vaginal normal y de la porción baja del tubo digestivo en 5 a 25% de las mujeres. La infección estreptocócica del grupo B durante el primer mes de vida puede presentarse como septicemia fulminante, meningitis o síndrome de dificultad respiratoria. La ampicilina intravenosa administrada a las madres, que son portadoras de estreptococos del grupo B y que están en trabajo de parto, evita la colonización en sus lactantes y la enfermedad por estreptococos del grupo B. Las infecciones por estreptococos del grupo B están aumentando en personas adultas no embarazadas, es decir los ancianos y los hospederos inmunodeprimidos, son los que tienen mas riesgo de enfermedad invasiva. Los factores predisponentes comprenden diabetes mellitus, cáncer, edad avanzada, cirrosis hepática, tratamiento con corticoesteroides, infección por VIH y otros estados de inmunodeficiencia. La bacteriemia, las infecciones de la piel y los tejidos blandos, las infecciones respiratorias y las infecciones genitourinarias en orden de frecuencia descendente constituyen las principales manifestaciones clínicas.
Patogenia (descripción, manifestaciones, diagnostico, tratamiento, prevención)
Meningitis neonatal: La meningitis neonatal se manifiesta con fiebre, irritabilidad, rechazo del alimento, vómitos, somnolencia en los bebés. En niños mayores se presenta cefalea intensa, molestia ocular, somnolencia, vómitos e irritabilidad. Aproximadamente en el 40% de los casos se presentan convulsiones.
Prevención y tratamiento: La vacunación es la mejor prevención de la meningitis, principalmente para niños menores de 2 años. Hasta que lleguen los resultados de bacteorología se debe inciar un tratamiento de antibiótico empírico. Estos antibióticos deben atravesar la barrera hematoencefálica y ser preferentemente bactericidas. El uso de una cefalosporina de 3ª generación o un aminoglucósido es una buena opción ante gérmenes desconocidos, si bien la asociación de ampicilina es obligada para cubrir Listerias, Enterococos y otros gram positivos.Ante la presencia de ventriculitis y/o abscesos cerebrales, que no hayan evolucionado bien con el tratamiento anterior, está indicada la administración de cloramfenicol.
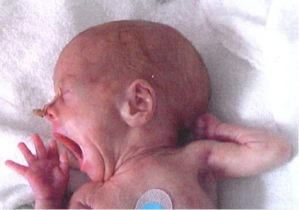
Septicemia: La septicemia se produce cuando existe una gran cantidad de agentes infecciosos en la sangre. Las infecciones por hongos y parásitos también pueden provocar esta afección. La infección inicial con frecuencia proviene de:
- Quemadura , úlcera u otra herida abierta
- Neumonía
- Infección de las vías urinarias
Las bacterias también pueden ingresar al torrente sanguíneo directamente desde una fuente exterior. Una aguja sucia utilizada por un consumidor de drogas intravenosas puede causar este tipo de infección. En algunos casos, se desconoce la fuente de la infección.
Cuando la afección se convierte en septicemia, los síntomas incluyen:
- Fiebre y escalofríos
- Temperatura baja
- Palidez de la piel
- Apatía
- Cambios en el estado mental
- Respiraciones aceleradas
- Incremento de la frecuencia cardíaca
- Disminución de la diuresis
- Baja presión arterial
- Choque
- Problemas de sangrado o coagulación
Prevención y tratamiento: No siempre es posible prevenir el envenenamiento de la sangre. Al evitar el abuso de drogas intravenosas, tiene menos probabilidades de sufrir septicemia. Los profesionales de la salud también deben implementar medidas para impedir la propagación de estas infecciones. La obtención de atención médica inmediata para tratar las infecciones puede disminuir el riesgo de septicemia.
Se puede realizar un tratamiento con penicilina ya que es muy sensible a el, pero se necesitan grandes cantidades para inhibir al microorganismo ya que ha generado una tolerancia y el microorganismo no se puede destruir.
Se recomienda la administración de penicilina G intravenosa 4 hrs. antes del parto
clindamicina o cefalosporina en las mujeres alérgicas a la penicilina, esto es para asegurara grandes cantidades de antibióticos en el torrente sanguíneo del neonato al momento del parto.
La administración de antibióticos durante la gestación resulta ineficaz para erradicar la colonización
vaginal, ya que, al suprimir el tratamiento, la vagina vuelve a colonizarse a partir del recto.
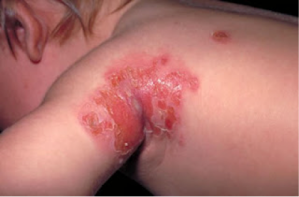
Epidemiologia
Sepsis y meningitis neonatal, la bacteria pasa del tubo digestivo a la vagina, la mortalidad es de 20% en neonatales.
Imágenes:
Streptococcus pneumoniae
Familia: Streptococcaceae
Genero: Streptococcus
Nombre científico: Streptococcus pneumonia
Nombre común: Neumococo
Fisiología microbiana: Los neumococos (Streptococcus pneumoniae) son diplococos grampositvos, a menudo de forma de lanceta o dispuestos en cadenas, poseen una capsula de polisacárido que permite la identificación con antisueros específicos. Los neumococos rápidamente experimentan lisis por compuestos con actividad en la superficie, lo cual probablemente elimina o inactiva a los inhibidores de las autolisinas de la pared celular. Los neumococos son residentes normales de las vías respiratorias altas de 5 a 40% de los seres humanos y pueden causar neumonía, sinusitis, otitis, bronquitis, bacteriemia, meningitis y otros procesos infecciosos.
Patogenia (descripción, manifestaciones, diagnostico, tratamiento, prevención)
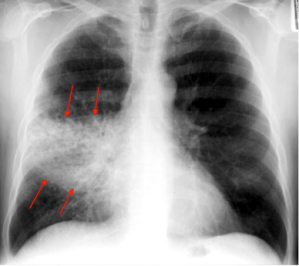
Neumonía: La neumonía causa inflamación en la vías respiratorias y causa que los sacos de aire de los pulmones se llenen de mucosa y otros líquidos, haciendo difícil que el oxígeno llegue a la sangre. La gente que está sana en otros sentidos se recupera rápidamente cuando se les da los cuidados apropiados con rapidez. Sin embargo, la neumonía es una condición seria. Los síntomas de la neumonía bacteriana incluyen: escalofríos, temblores y dolor en el pecho. Otros signos de la presencia de una neumonía bacteriana son: fiebre, respiración acelerada, aumento de la frecuencia cardiaca y dificultad para respirar.
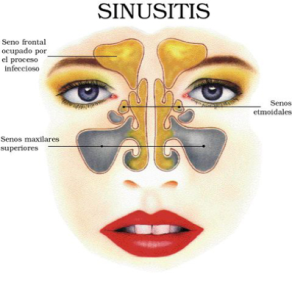
Sinusitis: La sinusitis bacteriana a veces se acompaña de odontalgia que suele afectar los molares superiores y también de halitosis (mal aliento). En la sinusitis aguda, el dolor espontáneo o la presión suele localizarse en el seno afectado (en particular el maxilar superior) y empeora cuando la persona flexiona la cintura hacia delante o está en decúbito dorsal. Las manifestaciones de sinusitis esfenoidal o etmoidal avanzada, a pesar de ser inusuales, tal vez sean intensas e incluyen dolor frontal o retroorbitario intenso que irradia al occipucio, trombosis del seno cavernoso y signos de celulitis orbitaria. La sinusitis focal aguda es poco común, pero hay que pensar en ella, por la afectación del seno maxilar superior y la fiebre en individuos con síntomas intensos, sea cual sea la duración de la enfermedad. De forma similar, el cuadro clínico inicial en individuos con sinusitis frontal avanzada puede comprender el llamado tumor congestivo de Pott en que hay hinchazón de partes blandas y edema blando sobre el hueso frontal, con un absceso subperióstico. Entre las complicaciones de la sinusitis que a veces son letales están la meningitis y los abscesos epidurales y cerebrales.
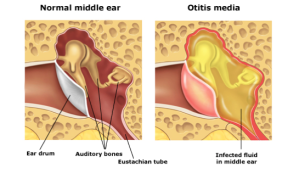
Otitis media: La otitis media es un trastorno inflamatorio del oído medio que aparece por disfunción de la trompa de Eustaquio, por diversas enfermedades, como URI y rinosinusitis crónica. La reacción inflamatoria a tales padecimientos hace que se genere un trasudado estéril dentro del oído medio y las cavidades mastoideas. El líquido puede infectarse si lo contaminan bacterias o virus que llegan de la nasofaringe y así produce un cuadro agudo (o a veces crónico).
Meningitis bacteriana: La meningitis bacteriana es una infección supurativa aguda localizada dentro del espacio subaracnoideo. Se acompaña de una reacción inflamatoria del sistema nervioso central (SNC) que puede producir disminución del nivel de conciencia, convulsiones, aumento de la presión intracraneal (ICP, intracranial pressure) y apoplejías. La reacción inflamatoria afecta meninges, espacio subaracnoideo y parénquima cerebral (meningoencefalitis). La terapia antimicrobiana de la meningitis por neumococos comienza con el uso de una cefalosporina (ceftriaxona, cefotaxima o cefepima) y vancomicina. En el caso de todas las cepas de S. pneumoniae aisladas en LCR se evaluará la sensibilidad a penicilina y cefalosporinas.
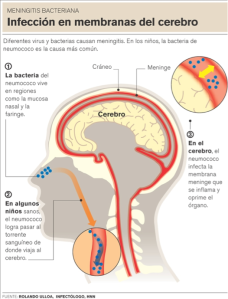
Tratamiento
Puesto que los neumococos son sensibles a muchos antimicrobianos, el tratamiento inicial por lo general logra el restablecimiento rápido y la respuesta de anticuerpos al parecer tiene una participación muy reducida. La penicilina G es el fármaco de elección. La penicilina G en dosis altas con MIC de 0.1 a 2 microgramos por mililitro al parecer es eficaz en el tratamiento de la neumonía causada por neumococos pero no seria eficaz para tratar la meningitis originada por las mismas cepas. Algunas cepas resistentes a la penicilina son resistentes a la cefotaxima. Tambien se presenta resistencia a la tetraciclina y a la eritromicina. Los neumococos se mantienen suceptibles a la vancomicina.
Epidemiologia, prevención y control
La neumonía neumococica constituye casi 60% de todas las nuemonias bacterianas. En el desarrollo de la enfermedad, los factores predisponentes son mas importantes que la exposición al microorganismo infeccioso y el portador sano es mas importante para diseminar los neumococos que el paciente enfermo. Es posible inmunizar a las personas con polisacáridos específicos. Estas vacunas probablemente confieren una protección de 90% contra la neumonía bacteriana.
Imágenes:
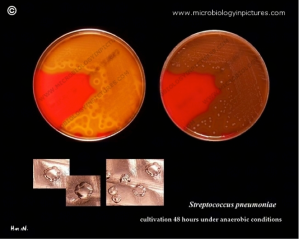
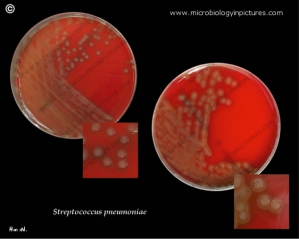
Fuentes:
Microbiología Medica,
De Jawetz, Melnick y Aldelberg.
D. R. 1999
Editorial El Manual Moderno, S. A de C. V
06100 México. D. F.
http://streptococcuspyogenes.blogspot.com
http://scielo.sld.cu/scielo.php?pid=S1561-30032013000200002&script=sci_arttext